Alcanos
Alcano é uma das classificações para os vários tipos de hidrocarbonetos que existem. São substâncias constituídas por carbonos e hidrogênios, unidos por ligação do tipo covalente, o que faz com que as moléculas da função alcano sejam pouco reativas. São insolúveis em água, e o ponto de fusão, o de ebulição e o estado físico da substância variam conforme o tamanho da cadeia carbônica em cada molécula.
A principal fonte de obtenção dos alcanos é o refino do petróleo e o processamento de gás natural. Os alcanos podem ser utilizados como combustível, solvente e matéria-prima para cosméticos, velas, entre outros produtos.
Leia também: Alcinos – compostos orgânicos de cadeia aberta, insaturados e de baixa densidade
Propriedades dos alcanos
-
Ponto de fusão e ebulição: são inferiores aos dos demais compostos orgânicos com mesma massa molecular e variam conforme o tamanho da cadeia.
Estado físico em condições normais de temperatura e pressão: alcanos com até 4 carbonos são gasosos; com 5 a 17 carbonos, são líquidos; com 18 ou mais carbonos, são sólidos. -
São insolúveis em água.
Os átomos da molécula de um alcano são conectados por ligações covalentes, que são ligações estáveis. Portanto, são compostos pouco reativos. -
São saturados, pois possuem apenas ligações simples (sigma – σ), e apresentam cadeia aberta (acíclicos).
-
Apresentam densidade menor que 1,0 g/m³.
Fórmula dos alcanos
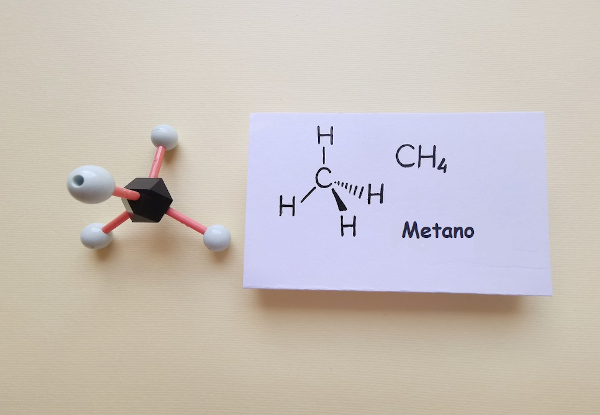
A fórmula geral para alcanos é: CnH2n+2. O “n” representa o número de carbonos presentes na cadeia.
Exemplo:
CH3-CH2-CH2-CH2-CH2-CH3
Fazendo a contagem apenas dos carbonos e usando a fórmula geral para alcanos, é possível obter a fórmula molecular desse composto:
C6H2*6+2 = C6H14.
Nomenclatura dos alcanos
A nomenclatura de alcanos segue as regras estabelecidas pela União Internacional da Química Pura e Aplicada (Iupac) e é composta por:
nome + posição da ramificação (se houver) + prefixo + an + o
Nome do radical e prefixo variam de acordo com o número de carbonos em cada um. O infixo “-an-” indica que a cadeia é saturada, ou seja, não possui duplas ou triplas ligações. Por último, o sufixo “-o” é característico de hidrocarbonetos, que é o tipo de molécula a que pertence a função alcano.
→ Prefixo
-
1 carbono = met-
-
2 carbonos = et-
-
3 carbonos = prop-
-
4 carbonos = but-
-
5 carbonos = pent-
-
6 carbonos = hex-
-
7 carbonos = hept-
-
8 carbonos = oct-
-
9 carbonos = non-
-
10 carbonos = dec-
→ Nome e posição da ramificação
Para indicar a posição da ramificação, devemos numerar a cadeia carbônica principal do alcano, começando sempre pelo lado mais próximo da ramificação. Assim, a localização da ramificação é o número do carbono ao qual ela está ligada. O nome dado ao radical será composto por prefixo (indicando quantos carbonos têm no radical) + il ou ila.
Quando houver mais de uma ramificação, deve-se usar ordem alfabética para posicioná-las na nomenclatura do composto. Caso sejam duas ou três ramificações iguais, é possível ainda usar “di-, -tri, -tetra...” antes do nome do radical.
Exemplos:
-
CH3-CH3 → Etano
-
CH3-CH2-CH3 → Propano
- CH3-CH2-CH2-CH2-CH3 → Pentano
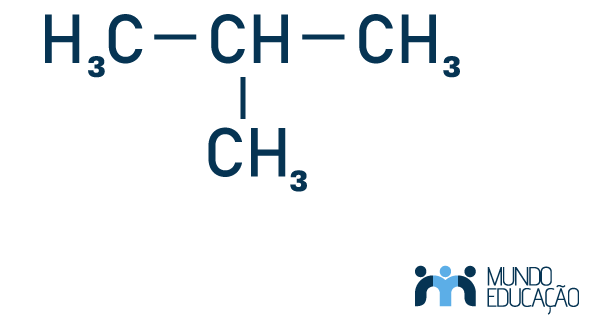
→ Metil-propano
Observe que nesse caso não há a indicação da posição da ramificação. Isso acontece porque essa informação torna-se desnecessária, pois não há outra posição para uma ramificação. Caso o metil estivesse no carbono 1, ele não seria um radical, e sim continuação da cadeia principal.
→ 4-etil-2-metil-hexano
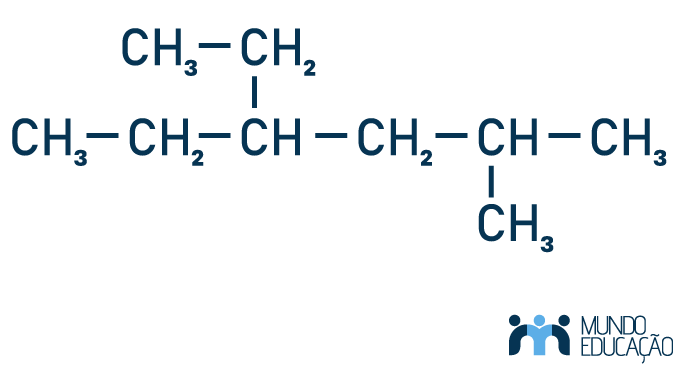
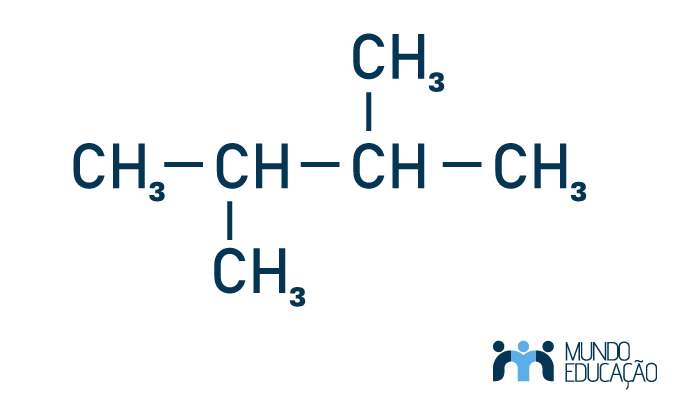
Nesse caso há duas ramificações. Perceba que a contagem foi feita da direita para a esquerda, de forma que os numerais que aparecem na nomenclatura são os de menor valor.
→ 2,3 dimetil-butano
Para dois radicais iguais, ambos com um carbono, cabe o uso do “di”.
Leia também: Nomenclatura de hidrocarbonetos ramificados
Fontes de obtenção dos alcanos
A principal fonte de obtenção dos alcanos é o petróleo e o gás natural. O alcano que provém do petróleo aparece após o processo de refino, depois da destilação fracionada do petróleo bruto. Algumas frações do petróleo pertencem à função alcano, como a gasolina, parafina, gás butano, hexano, óleos, entre outros. O principal gás que é fonte de alcano é o metano, o qual é liberado por animais e em processos como a decomposição de matéria orgânica.

Aplicações dos alcanos
-
Fonte de energia: gás de cozinha (GLP), gás butano utilizado em isqueiro, combustível automotivo, como gasolina e diesel (há uma grande parcela de moléculas que são da função alcano), etc.
-
Solventes orgânicos: hexano.
-
Os alcanos que formam líquidos densos são usados como óleos lubrificantes.
-
Os alcanos sólidos são usados como matéria-prima na produção de velas, cosméticos e outros objetos com parafina. O nome parafina vem do latim (parum = pequena + affinis = afinidade) e indica uma das principais características dos alcanos: ser pouco reativo.

Exercícios resolvidos
Questão 1 - (UEL) – A fórmula molecular do 2,3-dimetil butano é:
A) C6H14
B) C6H12
C) C6H10
D) C4H10
E) C4H8
Resolução
Alternativa A. Analisando a nomenclatura do composto 2,3-dimetil butano, pode-se perceber pela terminação -ano que ele é um alcano; -but- significa que a cadeia principal possui 4 carbonos; e 2,3-dimetil faz referência a 2 radicais metil; um está no carbono 2, e o outro, no carbono 3. Montando, teremos a seguinte molécula:
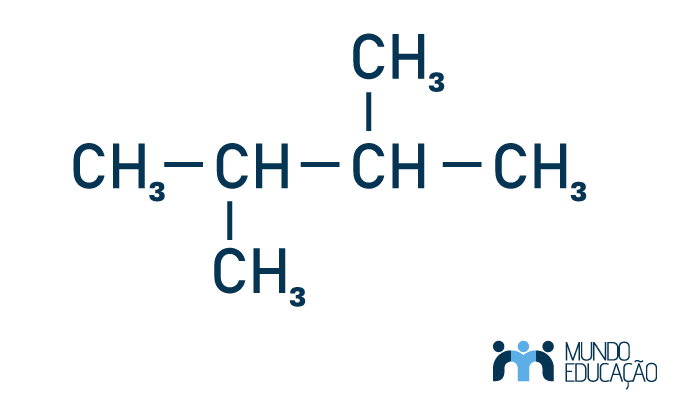
Fazendo a contagem dos carbonos ou indo direto pela análise da nomenclatura, sabemos que temos um total de seis carbonos na molécula. Usando a fórmula geral para alcanos CnH2n+2, teremos que a fórmula do 2,3-dimetil butano é C6H14.
Questão 2 - Considere as seguintes afirmações sobre os alcanos:
I – Os alcanos são compostos orgânicos constituídos por hidrogênio e carbono.
II – São moléculas saturadas, e os átomos realizam entre si ligações do tipo covalente.
III – Os alcanos podem ter moléculas de formação estrutural aberta (acíclica) ou fechada (cíclica).
IV – Os alcanos formam substâncias insolúveis em água.
A) Estão corretas I, II, III.
B) Estão incorretas II e IV.
C) Estão corretas I, II, IV.
D) Estão incorretas II, III e IV.
Resolução
Alternativa C. A afirmativa III está incorreta porque os compostos de cadeia fechada recebem outra classificação. Trata-se dos ciclanos.
Questão 3 - (Fatec) O gás liquefeito de petróleo, GLP, é uma mistura de propano, C3H8, e butano, C4H10. Logo, esse gás é uma mistura de hidrocarbonetos da classe dos:
A) alcanos.
B) alcenos.
C) alcinos.
D) cicloalcanos.
E) cicloalcenos.
Resolução
Alternativa A. O propano e o butano são alcanos, o que pode ser atestado pela terminação da nomenclatura. Perceba que ambos terminam em “ano”, que é o sufixo característico de hidrocarbonetos saturados, e não possuem a palavra “ciclo” precedendo a nomenclatura, o que configuraria um composto da função ciclano.
Artigos Relacionados

Últimas notícias
Outras matérias


















