Alotropia do Enxofre

O fenômeno da alotropia ocorre quando um mesmo elemento forma substâncias simples diferentes. Isso acontece com o carbono, com o fósforo, com o oxigênio e com o enxofre.
O enxofre possui a maior variedade de formas alotrópicas (S2, S4, S6 e S8), que podem ser encontradas, principalmente, em lugares propensos a ocorrer erupções vulcânicas. Porém, duas formas alotrópicas do enxofre se destacam, sendo que ambas possuem a fórmula S8, isto é, suas moléculas são formadas por oito átomos de enxofre ligados em forma de anel. A diferença está somente nas arrumações de suas moléculas no espaço.
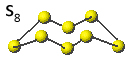
Veja as características de cada um:
- Enxofre Rômbico ou Enxofre α (alfa):
Essa é a forma alotrópica mais estável do enxofre e, portanto, a mais comum. Aparece na forma de cristais amarelos e transparentes, como se pode ver logo abaixo:

Seu ponto de fusão é igual a 112, 8ºC e seu ponto de ebulição é de 444,6ºC.
- Enxofre Monoclínico ou Enxofre β (beta):
Esse alótropo do enxofre apresenta-se na forma de agulhas finas e opacas, como mostra a figura abaixo. É menos estável que o enxofre rômbico, seu ponto de fusão é maior (119 ºC ) e possui o mesmo ponto de ebulição (444,6ºC).


Últimas notícias
Outras matérias


















