Produção de alumínio por eletrólise

O alumínio é um metal bastante utilizado em estruturas e em objetos em vários setores da sociedade, tais como na construção civil, nos transportes (como em carrocerias de automóveis, embarcações, fuselagens de aviões e em aros de bicicletas), em eletroeletrônica, na indústria petroquímica e metalúrgica, em tampas de iogurte, frigideiras, papel alumínio e assim por diante.

Ele tem essa ampla aplicação devido às suas propriedades, como baixa densidade, elevada resistência mecânica e à corrosão. Além disso, ele é muito usado em ligas metálicas, tais como o duralumínio (95,5% de alumínio, 3% de cobre, 1% de manganês e 0,5 de magnésio).
No entanto, o alumínio não aparece na sua forma elementar (Aℓ(s)) na natureza, apenas combinado com outros elementos formando compostos como os minérios. O principal minério que possui o alumínio é a bauxita, que contém óxido de alumínio hidratado (Aℓ2O3 . x H2O) e diversas impurezas. A foto abaixo mostra o minério bauxita natural e tubos feitos de alumínio metálico:

O processo que era feito antigamente para obter o alumínio a partir da alumina (Aℓ2O3) da bauxita era caro e ineficiente. Além do mais, a alumina possui ponto de fusão em cerca de 2 000 ºC, uma temperatura muito elevada.
Mas, em 1886, o americano Charles M. Hall e o francês Paul Héroult desenvolveram de modo independente um método que é usado até hoje para se produzir o alumínio a partir da alumina. Esse método, que se dá por meio da eletrólise, é chamado de Processo de Hall-Héroult, ou, simplesmente, Processo de Hall, visto que Charles M. Hall o patenteou.
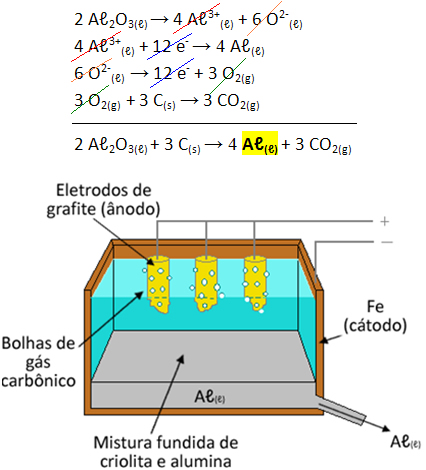
Eles descobriram que a criolita (Na3AℓF6) atua como fundente da alumina, isto é, a criolita consegue baixar o ponto de fusão da alumina a cerca de 1000 ºC. Assim, o processo de Hall-Héroult consiste em colocar a mistura fundida da alumina com a criolita (Aℓ2O3 + Na3AℓF6) num recipiente feito de ferro ou de aço (liga metálica cujo principal constituinte é o ferro), com eletrodos de carbono (pode ser de carvão ou de grafite) mergulhados nessa mistura. Visto que está fundida, a mistura líquida contém os íons Aℓ3+(ℓ) e O2-(ℓ) livres.
2 Aℓ2O3(ℓ) → 4 Aℓ3+(ℓ) + 6 O2-(ℓ)
O recipiente de aço atua como cátodo, ou seja, como polo negativo, onde ocorre a redução dos cátions do alumínio:
Semirreação do cátodo: 4 Aℓ3+(ℓ) + 12 e- → 4 Aℓ(ℓ)
Esse alumínio formado permanece no estado líquido, porque o seu ponto de fusão é menor que o da mistura “criolita+alumina”, sendo igual a 660,37 ºC. Porém, visto que sua densidade é maior que a densidade da mistura, ele desce para o fundo do recipiente, onde é coletado por escoamento.
Depois o alumínio fundido é colocado em moldes, nos quais se solidifica.

Os eletrodos de carbono atuam como ânodos, polos positivos onde há a oxidação dos ânions oxigênio:
Semirreação do ânodo: 6 O2-(ℓ) → 12 e- + 3 O2(g)
Esse gás oxigênio formado reage com o carbono do eletrodo e forma o gás carbônico (CO2(g)):
3 O2(g) + 3 C(s) → 3 CO2(g)
Desse modo, a equação global que ocorre nesse processo é dada por:
Artigos Relacionados

Últimas notícias
Outras matérias


















