Coloides ou Dispersões Coloidais
Quando misturamos um soluto num solvente, existem três tipos de dispersões que podem ser formadas: as soluções, os coloides e suspensões.
As soluções verdadeiras são homogêneas, isto é, conseguimos observar (a olho nu ou com um microscópio) uma única fase, pois o tamanho das partículas dispersas são menores que 1 nm. Além disso, não é possível separar seus componentes por meio de processos físicos, como uma filtração.
O oposto total são as suspensões, que são heterogêneas. Observamos duas fases ou mais, sendo que o tamanho das partículas dispersas é acima de 1000 nm e é possível separar seus componentes usando processos físicos, essas partículas podem ser retidas por um filtro.
Já os coloides são suspensões que se situam entre esses dois tipos de dispersões. A olho nu, achamos que o coloide é uma solução verdadeira, mas, com a ajuda de um microscópio, notamos que na verdade se trata de uma mistura heterogênea.
Por exemplo, o leite é um coloide no qual vemos apenas uma fase branca, mas, sob o olhar do microscópio, percebemos que existem gorduras dispersas na água.
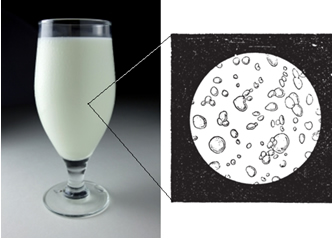
O tamanho das partículas dispersas nos coloides está entre 1 e 1000 nm e elas não se sedimentam sob ação da gravidade, mas ficam dispersas em toda a extensão da dispersão. Para separá-las, pode-se usar uma ultracentrífuga.
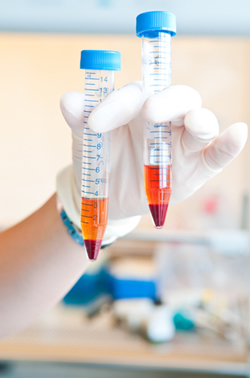
O sangue é outro exemplo de coloide. A seguir, temos uma amostra de sangue que a olho nu parece ser homogênea, mas no microscópio vemos os seus componentes. Na imagem introdutória deste texto, vemos que as suas partículas se sedimentaram com o uso da ultracentrífuga.
.jpg)
Uma das propriedades que os coloides apresentam é a de dispersar a luz que atravessa suas partículas. Entenda como isso acontece lendo o texto Efeito Tyndall.
Existem vários tipos de misturas que são dispersões coloidais, por isso foi feita uma classificação desses coloides de acordo com o tipo de solvente e soluto que o compõem. Segundo essa classificação, temos cinco tipos de coloides, que são:
1- Espuma: Gás disperso em sólido ou líquido. Exemplos: pedra-pome, clara em neve, chantilly, esponja.
2- Emulsão: Líquido disperso em outro líquido ou sólido. Exemplos: leite, maionese, queijo e manteiga.
3- Sol: Sólido disperso num líquido. Exemplos: sangue, rubis, pérolas e solução de goma.
4- Gel: Líquido disperso num sólido. Exemplos: gel de cabelo, gelatina.
5- Aerossol: Sólido ou líquido disperso em gás. Exemplos: fumaça, neblina, nevoeiros, spray e umidificador de ar.

Artigos Relacionados

Últimas notícias
Outras matérias


















