Como se formam as bolhas de sabão?

Crianças e até mesmo adultos em todo o mundo gostam de brincar com bolhas de sabão. Mas, você já se perguntou o que será que as formam? O que mantém suas moléculas unidas? Por que elas sempre são esféricas? Como fazer para conseguir bolhas de sabão mais resistentes?
As respostas para todas essas perguntas se baseiam no tipo de força intermolecular existente entre as moléculas de água: a ligação de hidrogênio. Essas ligações ocorrem na água pela atração do polo positivo de uma molécula (hidrogênio) com o polo negativo de outra (oxigênio).
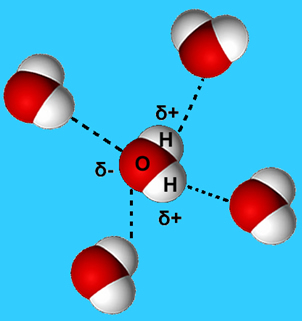
Essas interações ocorrem em todas as direções, no entanto, elas se tornam ainda mais intensas na superfície da água, pois como não existem moléculas na parte de cima, somente dos lados e abaixo, a desigualdade de atrações provoca a contração do líquido, dando a impressão de existir uma fina película na sua superfície. Esse fenômeno é chamado de tensão superficial.
As bolhas se formam graças à intensidade dessa tensão superficial. As moléculas de água que estão na superfície da bolha realizam ligações de hidrogênio somente com moléculas ao seu lado, aumentando ainda mais a força dessa ligação. Para diminuir essa superfície ao mínimo, a bolha adquire um formato com a menor relação entre área superficial e volume, que é a forma esférica.

As moléculas do detergente se interpõem às moléculas de água. A elasticidade é resultante da interação entre as moléculas de água restantes. No entanto, elas acabam por evaporar e, como consequência, a bolha estoura.
Mas, se você quiser aumentar a resistência das bolhas de sabão, basta acrescentar qualquer produto formado por substâncias que contenham o grupo OH em suas moléculas. Dessa forma, se estabelecerá ligações de hidrogênio com a água e ela permanecerá por mais tempo no estado líquido. Exemplos de substâncias assim são o açúcar (sacarose), a glicerina, a glicose e a frutose. Algo que dá certo é adicionar xarope de milho à mistura de água e detergente, porque ele é constituído basicamente de 20% de glicose e 80 % de frutose.

Artigos Relacionados

Últimas notícias
Outras matérias


















