Geometria tetraédrica

Geometria tetraédrica é uma forma de geometria molecular, ou seja, uma maneira como os átomos de uma molécula estão organizados no espaço. As moléculas com geometria molecular seguem um padrão, de acordo com as regras propostas por Gillespie:
-
Moléculas com cinco átomos;
-
Átomo central ligado a quatro átomos iguais ou diferentes;
-
O átomo central nunca apresenta elétrons não ligantes, ou seja, todos os elétrons da sua camada de valência são utilizados em ligações;
-
O átomo central é aquele que apresenta a capacidade de fazer o maior número de ligações (geralmente, elemento químico que pertence às famílias IVA e VA) para atingir a regra do octeto;
-
Átomo central realiza quatro ligações.
Veja alguns exemplos de moléculas que apresentam geometria tetraédrica:
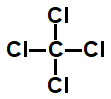
Tetracloreto de carbono (CCl4)
Podemos destacar nessa molécula:
-
O carbono é átomo central;
-
4 átomos de cloro ligados ao átomo central;
Não pare agora... Tem mais depois da publicidade ;) -
Átomo central (carbono) com quatro elétrons na camada de valência, já que pertence à família IV A;
-
4 ligações entre o carbono e os átomos de cloro (as ligações são simples porque o átomo de cloro só necessita de uma ligação para atingir o octeto);
-
Nenhum elétron não ligante no átomo central (todos os elétrons da camada de valência do carbono estão sendo utilizados nas ligações com os átomos de cloro).
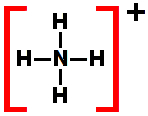
Cátion amônio (NH4+)
Podemos destacar nessa molécula:
-
O nitrogênio é o átomo central;
-
4 átomos de hidrogênio ligados ao átomo central;
-
Nitrogênio apresente cinco elétrons na camada de valência, já que pertence à família V A;
-
Há três ligações simples e uma ligação dativa entre o nitrogênio e os átomos de hidrogênio
-
Nenhum elétron não ligante no átomo central.
Artigos Relacionados

Últimas notícias
Outras matérias