Halogenação de alcanos
Halogenação de alcanos é o nome dado à reação orgânica de substituição, que ocorre sempre que essa subclasse dos hidrocarbonetos (as outras são os alcenos, alcinos, alcadienos, ciclanos, ciclenos e aromáticos) é colocada em um mesmo recipiente que um halogênio molecular (cloro-Cl2, iodo-I2 ou bromo-Br2). A representação geral dos halogênios é X2.
Obs.: A reação de halogenação de alcanos com flúor (F2) não é realizada por ser um processo explosivo e tem como principal característica a destruição da matéria orgânica.
Mesmo estando o alcano e o halogênio no mesmo recipiente, trata-se de uma reação química que necessita de um catalisador para ocorrer de uma forma mais rápida, já que, em geral, esse processo aconteceria lentamente por causa da característica pouco reativa dos alcanos. O catalisador utilizado em uma halogenação é a luz (λ) ou o calor (∆).
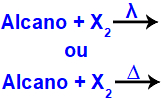
Representação dos reagentes de uma halogenação
A reação de halogenação de alcanos ocorre por substituição, pois, nesses compostos, há apenas a presença de ligações do tipo sigma entre os carbonos, como também entre os carbonos e os hidrogênios. A ligação entre carbono e hidrogênio é mais instável, ou seja, mais fácil de ser rompida, por causa da diferença de eletronegatividade.
Mecanismos da halogenação de alcanos
Destacamos a seguir os passos que ocorrem durante uma reação de halogenação de alcanos:
-
1º Passo: quebra no halogênio
Inicialmente, acontece a quebra da ligação sigma entre os dois átomos de halogênio, liberando-os na forma de radicais livres:
![]()
Rompimento da ligação sigma entre os halogênios
-
2º Passo: Ataque dos radicais livres
Os radicais livres atacam a cadeia carbônica no local de maior diferença de eletronegatividade, quebrando a ligação sigma entre o hidrogênio e o carbono. Assim, haverá um hidrogênio radicalar livre e um radical orgânico.
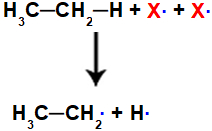
Rompimento da ligação sigma entre o carbono e o hidrogênio
-
3º Passo: Formação dos produtos
Por fim, um dos halogênios, na forma de radical, interage com o carbono do radical orgânico, enquanto o outro halogênio interage com o hidrogênio:
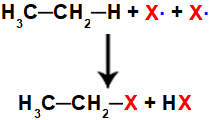
Equação representando a formação dos produtos
Os produtos formados em toda reação de halogenação de alcanos são haletos orgânicos e hidrácido inorgânico.
Variações dos produtos nas reações de halogenação em alcanos
Quando avaliamos a halogenação no metano, verificamos quatro ligações sigma iguais entre quatro hidrogênios e um carbono, ou seja, a quebra de qualquer uma delas será feita de forma igual.
Quando o alcano apresenta um número maior de carbonos, passamos a ter carbonos com quantidades diferentes de hidrogênios. Portanto, quando os halogênios radicalares atacam as moléculas de alcanos presentes no meio, são formados radicais diferentes.
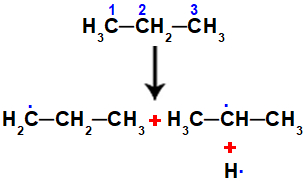
Possíveis radicais formados a partir do propano
Nota-se no propano que os carbonos 1 e 3 são iguais, pois apresentam a mesma quantidade de hidrogênios e estão ligados ao mesmo carbono e, por isso, têm a mesma estabilidade. O carbono 2, entretanto, é diferente deles, por isso, a partir desse alcano, podem ser formados dois radicais, o que resultaria na formação de dois produtos diferentes na reação de halogenação.
Assim, quanto mais estável (com menor número de hidrogênios) for o carbono, maior a probabilidade de quebra da ligação sigma entre o hidrogênio e o carbono. Essa estabilidade está relacionada com o tipo de carbono presente na cadeia, ou seja, quanto maior o número de carbonos ligados a um mesmo carbono, mais estável ele será, de acordo com a ordem decrescente abaixo:
Terciário > Secundário > Primário
Exemplo: 2-metil-butano
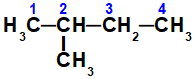
Fórmula estrutural do 2-metil-butano
Nesse alcano, há cinco átomos de carbono, sendo que quatro deles (1, 2, 3 e 4) são diferentes uns dos outros, ou seja, apresentam estabilidades diferentes. Assim, durante essa reação de halogenação, haverá a formação de quatro radicais orgânicos.
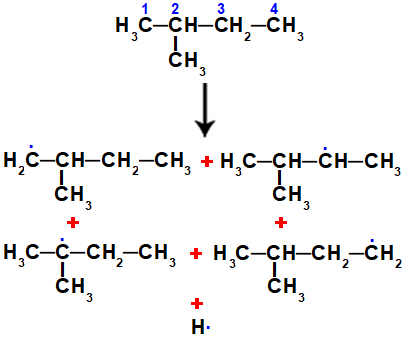
Possíveis radicais orgânicos formados a partir do 2-metil-butano
Obs.: O carbono 1 não é igual ao carbono 4, porque esses carbonos estão ligados a carbonos de estabilidades diferentes e, por essa razão, formam radicais diferentes.
Dessa forma, se o 2-metil-butano for submetido a uma reação de bromação (Br2), serão formados quatro haletos orgânicos diferentes, sendo o 2-bromo-2-metil-butano o produto principal, por ter sido originado a partir do radical com a valência no carbono terciário:
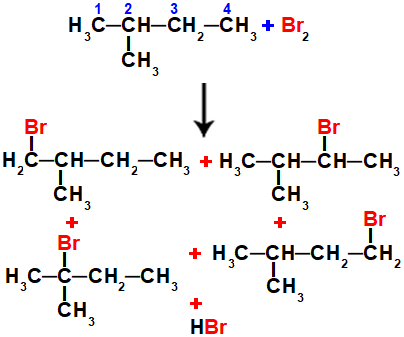
Possíveis produtos orgânicos formados a partir do 2-metil-butano
Artigos Relacionados

Últimas notícias
Outras matérias







.jpg)











