Isomeria Dinâmica ou Tautomeria

A palavra tautomeria vem de tautos, que significa “dois de si mesmo” e meros, “partes”. Assim, esse tipo de isomeria só ocorre em soluções, isto é, somente na fase líquida e em compostos cuja molécula possui um elemento muito eletronegativo, como o oxigênio e o nitrogênio.
O que ocorre é que uma dupla ligação carbono-oxigênio ou carbono-nitrogênio pode ser deslocada para o átomo de carbono vizinho e as substâncias envolvidas estabelecem um equilíbrio dinâmico.
Os dois casos principais de isomeria dinâmica ou tautomeria são os explanados abaixo:
1. Tautomeria aldoenólica: nesse caso, coexistem em equilíbrio dinâmico um aldeído e um enol (composto instável que possui o grupo hidroxila (OH) ligado a um carbono insaturado).
Por exemplo, em uma solução de aldeído acético ocorre que uma pequena parte se transforma em etenol, que, por sua vez, regenera o aldeído e é estabelecido um equilíbrio. Conforme mostra essa reação abaixo, isso acontece porque o átomo de hidrogênio do carbono vizinho migra para o oxigênio da carbonila, produzindo uma substância que pertence à outra função, que no caso é um enol.
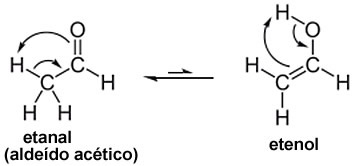
Depois que o eteno é formado, a alta eletronegatividade do oxigênio atrai fortemente os elétrons da dupla ligação que o carbono realiza, que é uma ligação fraca e fácil de deslocar. Por isso, o etanal é regenerado e as duas substâncias passam a existir em equilíbrio dinâmico.
Porém, o equilíbrio está deslocado para a direita, ou seja, para a formação do aldeído, que estará presente no meio em maior quantidade que o enol. Isso ocorre porque o caráter ácido do hidrogênio do carbono 2 do aldeído é menor que o caráter ácido do hidrogênio do grupo hidroxila do enol. Portanto, o aldeído libera o átomo de hidrogênio com menor intensidade que o enol, e a reação ocorre mais intensamente para a esquerda.
2. Tautomeria cetoenólico: essa tautomeria se dá entre cetonas e enóis em meio aquoso.
O princípio de funcionamento é o mesmo que o explicado no item anterior; veja um exemplo:
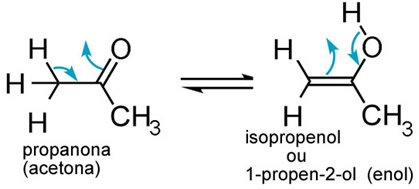
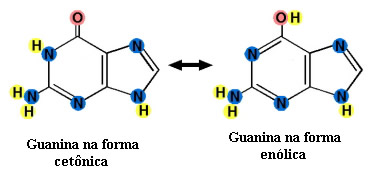
A tautomeria é muito importante nas formações cetoenólicas da guanina, que é uma das quatro bases nitrogenadas que compõem o DNA. A guanina sempre se emparelha com a citosina, na formação da dupla-hélice do DNA.
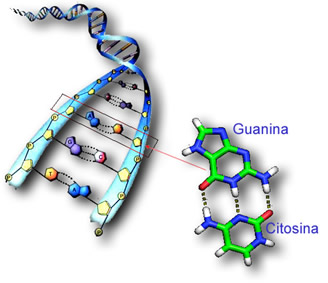
Veja a seguir o equilíbrio dinâmico que é estabelecido entre suas formas cetônica e enólica:
Artigos Relacionados

Últimas notícias
Outras matérias


















