O gelo que pega fogo

Você já viu na televisão ou na internet cenas iguais às mostradas abaixo, nas quais se coloca fogo no gelo da neve ou mesmo na água de rios?

Como podemos explicar esse fato? E mais especificamente: como o gelo pega fogo?
Bom, o composto com aparência de gelo que pega fogo, nesses casos, é o hidrato de metano. Ele é formado por moléculas do gás metano (CH4) contidas numa espécie de “gaiola” de água congelada. Essa estrutura é mostrada a seguir:
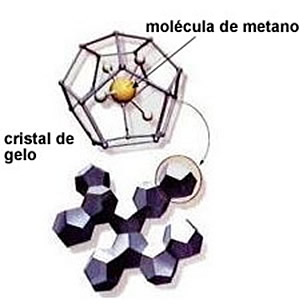
O hidrato de metano é formado principalmente no fundo de oceanos, onde materiais orgânicos entram em decomposição e, dessa forma, os microrganismos sintetizam, entre outros compostos, o metano. Esse gás é então liberado, sendo que parte dele é encapsulada pelos cristais de gelo, produzindo o hidrato de metano em camadas de água de aproximadamente 500 metros.
Na temperatura próxima ao congelamento da água, o hidrato de metano permanece de forma estável. No entanto, à temperatura ambiente, ele se decompõe rapidamente, liberando o gás metano. É por isso que ele pega fogo facilmente, seja no gelo, seja em rochas ou até mesmo na água de rios.
No caso de certos rios, esse fenômeno se deve ao fato de que uma enorme quantidade de matéria orgânica da floresta ao redor cai e se deposita no fundo do rio. Depois, ela se decompõe e gera o gás metano. Ele é liberado lentamente, produzindo bolhas na superfície do rio. Quando há uma movimentação no fundo do rio, a produção de bolhas aumenta e é possível colocar fogo no gás que queima enquanto houver mais gás aflorando na superfície.
Nas ilustrações abaixo há amostras de hidratos de metano retirados pela mineração de rochas com lama. Na primeira imagem você pode ver as bolhas de ar do metano saindo, pois o gelo começou a derreter:
.jpg)
Para que a amostra seja preservada, é necessário guardá-la em recipientes fechados e resfriados com nitrogênio líquido (N2).
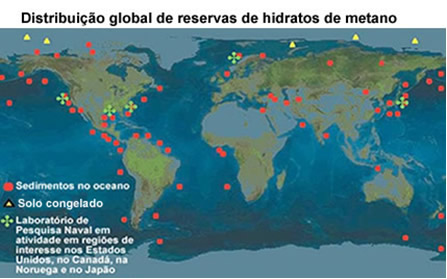
Os depósitos desse material se concentram principalmente ao longo dos oceanos do hemisfério Norte. Visto que ele contém energia armazenada, estudos estão sendo feitos para descobrir como ele pode ser usado na geração de energia no futuro. Entretanto, essa alternativa energética pode causar sérios danos ao meio ambiente, pois o escape de metano para a atmosfera, provocado pelo processo de extração, aumentaria o efeito estufa e o aquecimento global. Além disso, o metano na presença de oxigênio livre produz o dióxido de carbono (CO2 – gás carbônico), que é o principal causador do efeito estufa.
Artigos Relacionados

Últimas notícias
Outras matérias


















