Reações de Análise ou Decomposição

As reações de análise também chamadas de reações de decomposição são aquelas em que um reagente composto (formado por mais de um tipo de elemento) é dividido em duas ou mais substâncias de estruturas simples (formadas por um único tipo de elemento).
De modo genérico, temos:
AB → A + B
Exemplo:
2 NaN3(s) → 3 N2(g) + 2 Na (s)
Essa é a reação que faz os airbags dos carros funcionarem e salvarem vidas. Dentro deles há a azida de sódio (NaN3), e quando há uma batida, um dispositivo dos airbags é acionado e a temperatura faz com que a azida se decomponha no gás nitrogênio e no sódio metálico.
O gás nitrogênio é um gás inerte que faz a bolsa (bag) inflar. O sódio pode ser reativo, por isso, outro composto é colocado dentro da bolsa, o nitrato de potássio, que reage com o sódio e gera mais gás nitrogênio. Essa segunda reação, no entanto, não é de decomposição ou análise.
Vários fatores podem causar a decomposição de um composto, entre eles, vamos destacar três:
- Calor: Quando algumas substâncias compostas são submetidas ao aquecimento, elas se decompõem. Esse tipo de reação é chamado de pirólise, que do grego piro significa “fogo” e lise significa “quebra”, isto é, quebra de um composto por meio do fogo.
Quando essa reação é feita na indústria, é também chamada de calcinação.
Um exemplo muito importante do uso da pirólise é na produção do bio-óleo ou alcatrão pirolítico, que é considerado uma alternativa energética para os combustíveis derivados do petróleo. A vantagem do bio-óleo é que ele não possui metais pesados como chumbo e mercúrio, que podem poluir o meio ambiente e contaminar seres vivos; não possui enxofre, que sofre reações na atmosfera e gera as chuvas ácidas, e também libera menos cinzas.
Outros exemplos de reações de decomposição pela ação do calor:
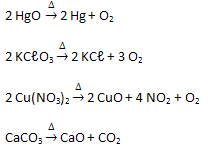
- Luz: A luz pode causar a decomposição dos compostos. Esse tipo de reação é chamado de fotólise.
Um exemplo é a água oxigenada que deve ser guardada em frascos escuros ou opacos, como o mostrado abaixo, para impedir a passagem de luz e a sua decomposição, produzindo água e gás oxigênio:

- Eletricidade: Ao passar uma corrente elétrica sobre um líquido ou um composto fundido, ele é decomposto em substâncias simples. Esse processo é chamado de eletrólise, que pode ser aquosa ou ígnea.
Um exemplo muito importante é a eletrólise ígnea do sal fundido (em que os seus íons Na+ e Cl- ficam livres). Ao passar a corrente elétrica por ele, originam-se duas substâncias simples importantes: o sódio metálico e o gás cloro.

Abaixo temos um esquema dessa eletrólise:
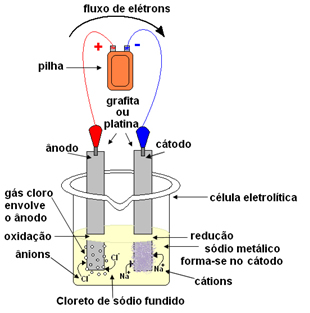
Outro exemplo é a eletrólise da água, que produz gás hidrogênio e gás oxigênio:

Artigos Relacionados

Últimas notícias
Outras matérias


















