Sal ácido

Um sal ácido é toda substância inorgânica formada obrigatoriamente por dois cátions, sendo um deles o hidrônio, representado por H+ ou H3O+, e o outro é um ânion qualquer (oxigenado ou não).
A formação de um sal ácido acontece por meio de uma reação de neutralização parcial de um ácido e uma base, processo no qual a quantidade de hidroxilas presentes na base não neutraliza todos os hidrogênios do ácido.
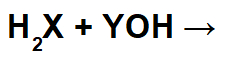
Equação de neutralização parcial
Analisando a equação acima, observa-se que o ácido genérico é binário, ou seja, possui dois hidrogênios, enquanto a base apresenta apenas uma hidroxila. Logo, nessa neutralização, uma hidroxila une-se a apenas um hidrogênio, formando a água:
.jpg)
Equação que representa a formação da água em uma neutralização
Já o cátion da base (Y+) interage com o hidrônio (H+) e o ânion do ácido (X-2), formando o sal ácido.
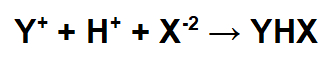
Equação representando a formação do sal ácido
Obs.: o ânion do ácido é bivalente
Por causa do hidrônio na fórmula de um sal ácido, para realizar sua nomenclatura, devemos levar em conta a seguinte regra:
Prefixo + hidrogeno + nome do ânion + de + nome do cátion
Exemplos
-
NaHCO3
Esse sal é gerado a partir da neutralização parcial entre o ácido carbônico (H2CO3) e o hidróxido de sódio (NaOH). A água é formada pela interação de um hidrônio (H+) com um hidróxido (OH-), e o sal é formado pela interação entre o cátion da base (Na+), o ânion (CO3-2) do ácido e o cátion hidrônio:
![]()
Equação de neutralização do ácido carbônico e hidróxido de sódio
Nesse sal ácido, temos os seguintes componentes:
- Cátion sódio: Na+
- 1 cátion hidrônio: mono
- Ânion carbonato: CO3-2
Logo, o nome desse sal é mono-hidrogeno-carbonato de sódio ou carbonato ácido de sódio.
-
CuHSO4
Esse sal é originado a partir da neutralização parcial entre o ácido sulfúrico (H2CO4) e o hidróxido de cobre I (CuOH). A água é formada pela interação de um hidrônio (H+) com um hidróxido (OH-), e o sal é formado pela interação entre o cátion da base (Cu+), o ânion (SO4-2) do ácido e o cátion hidrônio:
![]()
Equação de neutralização do ácido sulfúrico e hidróxido de cobre I
Nesse sal ácido, temos os seguintes componentes:
- Cátion cobre I: Cu+
- 1 cátion hidrônio: mono
- Ânion sulfato: SO4-2
Logo, o nome desse sal é mono-hidrogeno-sulfato de cobre I ou sulfato ácido de cobre I.
Artigos Relacionados

Últimas notícias
Outras matérias


















