Variação da entalpia e Lei de Hess
Conforme explicado no texto Lei de Hess, o médico e químico suíço Germain Henri Hess (1802-1850) determinou que a variação de entalpia (?H), isto é, o calor absorvido ou liberado em uma reação química, sob certas condições experimentais, depende exclusivamente da entalpia (conteúdo de energia) dos reagentes e dos produtos. Isso significa que, independentemente se a reação é executada em uma única etapa ou se ela é realizada em várias etapas sucessivas, o valor da variação de entalpia será o mesmo.
Essa lei é importante porque se não soubermos o ?H de determinada reação direta, mas soubermos os valores de ?H de outras reações que resultam na primeira, então podemos trabalhar com elas para descobrir o valor que queremos.
No entanto, muitas dúvidas surgem sobre como trabalhar com conjuntos de equações termoquímicas como se fossem equações matemáticas, por isso este artigo pretende explicar sobre os principais pontos que devem ser lembrados e as principais etapas que devem ser seguidas para realizar uma soma de equações sem erros.
Para tal, vejamos um exemplo:
“Observe o conjunto de equações abaixo:
C2H4(g) + 3 O2(g) → 2 CO2(g) + 2 H2O(?) ?H = - 1409,5 kJ
C(grafita) + O2(g) → CO2(g) ?H = - 393,3 kJ
H2(g)+ ½ O2(g) → H2O(?) ?H = - 285,5 kJ
Com base nessas equações e aplicando a Lei de Hess, vamos descobrir o valor da variação de entalpia da formação do acetileno na reação direta abaixo:
2 C(grafita) + 2 H2(g) → C2H4(g) ?H = ?”
* Em primeiro lugar, é preciso observar a equação em questão e ver quais são as substâncias que estão nos reagentes e quais estão nos produtos. Depois comparamos com o conjunto de equações acima e vemos se eles estão do mesmo lado. Se estiverem, mantemos a equação exatamente como está, mas se não estiverem, teremos que invertê-la.
Por exemplo, observe que o acetileno (C2H4(g)) deve ficar como produto, mas na primeira equação ele está como reagente, então teremos que inverter essa equação. Os reagentes C(grafita) e H2(g) estão do lado correto e, portanto, as equações 2 e 3 mantêm-se normais. Note abaixo como isso é feito:
2 CO2(g) + 2 H2O(?)→ C2H4(g) + 3 O2(g) ?H = + 1409,5 kJ
C(grafita) + O2(g) → CO2(g) ?H = - 393,3 kJ
H2(g)+ ½ O2(g) → H2O(?) ?H = - 285,5 kJ
* Agora, um ponto importantíssimo: não se esqueça de inverter também o valor do ?H, ou seja, se ele é positivo, ficará negativo e vice-versa. Isso foi feito acima.
* Outro ponto a ser levado em consideração é que, visto que pretendemos anular algumas substâncias que não fazem parte da equação que estamos trabalhando, precisamos satisfazer os coeficientes estequiométricos para tal, isto é, a quantidade dessas substâncias deve ser a mesma nos reagentes e nos produtos, para que, quando somarmos as equações, as somas dessas substâncias sejam iguais a zero. Com essa mesma finalidade, observamos se os coeficientes das substâncias da equação de referência são os mesmos que aparecem para elas no conjunto de equações.
Se esses fatores não estiverem sendo satisfeitos, precisaremos acertar os coeficientes e geralmente isso é feito por multiplicar a equação por algum número inteiro pequeno e positivo, geralmente, 2 ou 3. Quando for preciso fazer isso, não se esqueça de multiplicar também o valor do ?H.
No caso da equação acima, a água (H2O(?)), o dióxido de carbono (CO2(g)) e o oxigênio (O2(g)) não participam da reação que queremos, por isso deve haver a mesma quantidade dessas substâncias nos dois membros. Veja que, na primeira equação, temos 2 mol de H2O(?); enquanto, na terceira equação, temos apenas 1 mol. Por isso, teremos que multiplicar a terceira equação por 2. Ao fazermos isso, estaremos ao mesmo tempo resolvendo outros dois fatores: haverá 1 mol de O2(g) para que, quando for somado, dê o total de 3 mols, além de acertarmos também o coeficiente do H2(g), visto que, na equação de referência, temos 2 mols desse gás.
H2(g)+ ½ O2(g) → H2O(?) ?H = - 285,5 kJ . (2)
2 H2(g)+ 1 O2(g) → 2 H2O(?) ?H = - 571 kJ
Além disso, na equação que estamos procurando, o coeficiente da grafita é igual a 2, então vamos multiplicar também a segunda equação por 2:
C(grafita) + O2(g) → CO2(g) ?H = - 393,3 kJ. (2)
2 C(grafita) + 2 O2(g) → 2 CO2(g) ?H = - 786,6 kJ
Agora sim podemos somar essas equações, levando em conta que:
-
Se a quantidade da substância no regente é igual à do produto → zero (anula a substância);
-
Se a quantidade da substância no regente é maior que no produto → subtrai e o resultado fica no reagente;
-
Se a quantidade da substância no regente é menor que no produto → subtrai e o resultado fica no produto;
-
Se a substância aparece em mais de uma equação e de um mesmo lado, basta somá-los e colocar o resultado na equação final do mesmo lado;
-
Se a substância aparece apenas em uma única equação, somente se repete na equação final exatamente a mesma quantidade e o mesmo lado da equação.
Sabendo de tudo isso, vamos finalmente somar as equações e não se esqueça do ?H:
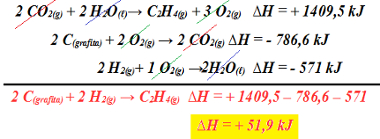
Desse modo, descobrimos o valor da variação de entalpia na reação direta que estávamos procurando.
Artigos Relacionados

Últimas notícias
Outras matérias


















